本期着重对药品包装材料生产洁净室(区)要求及检测方法进行详细阐述。
国家食品药品监督管理总局于2004年07月20发布《直接接触药品的包装材料和容器管理办法》(局令第13号),本办法自公布之日起施行。为加强直接接触药品的包装材料和容器(以下简称“药包材”)的监督管理,保证药包材质量,根据《中华人民共和国药品管理法》(以下简称《药品管理法》)及《中华人民共和国药品管理法实施条例》,制定本办法。
2015年8月11日国家食品药品监督管理局发布YBB00412004-2015《药品包装材料生产厂房洁净室(区)的测试方法》并于2015年12月1日实施,药品包装材料生产厂房洁净室(区)的检测方法依据该标准执行。
1、要求:
1.1 机构和人员要求:
1.1.1 药包材生产企业应建立与产品生产要求相适应的生产和质量管理机构。各级机构和人员职责应明确,并配备一定数量的与药包材生产相适应的具有专业知识、生产经验及组织能力的管理人员和技术人员。
1.1.2 主管药包材生产管理和质量管理的负责人应具有与所生产的产品相关专业知识,有该类产品生产和质量管理经验,对《通则》的实施和产品质量负责。
1.1.3 药包材生产管理部门和质量管理部门的负责人应具有相关专业中专以上学历,有该类产品生产和质量管理经验。有能力对药包材生产和质量管理中的实际问题作出正确的判断和处理。
1.1.4 药包材生产管理部门和质量管理部门负责人不得互相兼任。
1.1.5 从事药包材生产操作和质量检验的人员应经专业技术培训,具有基础理论知识和实际操作技能。
1.2 厂房与设施要求:
1.2.1 药包材生产企业必须有整洁的生产环境;厂区的地面、路面及运输等不应对产品造成污染;生产、管理、生活和辅助区域的总体布局应合理,不得互相妨碍,厂区内主要道路应宽敞、路面平整、并选择不易起尘的材料。厂区设计建造应符合国家有关规定。
1.2.2 厂房应按生产工艺流程及所要求的空气洁净度级别进行合理布局。同一厂房内以及相邻厂房之间的生产操作不得互相妨碍。
1.2.3 厂房应有防尘、防污染、防止昆虫和其他动物及异物进入的设施。
1.2.4 在设计和建设厂房时,应考虑(使用时)便于进行清洁工作。洁净室(区)的内表面应平整光滑、无裂缝、接口严密、无颗粒物脱落,并能耐受清洗和消毒,墙壁与地面的交界处宜成弧形或采取其他措施,以减少灰尘积聚和便于清洁。
1.2.5 生产区和储存区应有与生产规模相适应的面积和空间用以安装设备、物料,便于生产操作,存放物料、中间产品、待验品和成品,应最大限度地减少差错和交叉污染。
1.2.6 进入洁净室(区)的空气必须净化。生产不洗即用药包材,自成品成型(包括成型)以后各工序其洁净度要求应与所包装的药品生产洁净度相同,据此要求,药包材生产洁净室(区)的空气洁净度划分为四个级别(详见“洁净室(区)空气洁净度级别表”)。
表1洁净室(区)空气洁净度级别表
洁净度级别 | 尘埃最大允许数/立方米 | 微生物最大允许数 | 换气次数 | ||
≥0.5μm | ≥5μm | 浮游菌/立方米 | 沉降菌/皿 | ||
100 | 3500 | 0 | 5 | 1 | 垂直层流≥0.3米/秒 水平层流≥0.4米/秒 |
10000 | 350000 | 2000 | 100 | 3 | ≥20次/时 |
100000 | 3500000 | 20000 | 500 | 10 | ≥15次/时 |
300000 | 10500000 | 60000 | — | 15 | ≥12次/时 |
1.2.7 洁净室(区)与非洁净室(区)之间必须设置缓冲设施,人、物流走向合理。
1.2.8 洁净室(区)应根据生产要求提供足够的照明。主要工作室的照度宜为300勒克斯;对照度有特殊要求的生产部位可设置局部照明。厂房应有应急照明设施。
1.2.9 洁净室(区)的窗户、天棚及进入室内的管道、风口、灯具与墙壁或天棚的连接部位均应密封。空气洁净级别不同的相邻房间之间的静压差应大于5帕,洁净室(区)与室外大气的静压差应大于10帕,洁净室(区)与非洁净室(区)的静压差应大于5帕,并应有指示静压差的装置。
1.2.10 洁净室(区)的温度和相对湿度应与药包材生产工艺相适应。无特殊要求时,温度宜控制在18~26℃,相对湿度控制在45~65%。
1.2.11 洁净室(区)在静态条件下检测尘埃粒子数、浮游菌数或沉降菌数必须符合规定,应定期监控动态条件下的洁净状况。实时监控换气次数、静压差等参数。所有监测结果均应记录存档。
1.2.12 洁净室(区)内安装的水池、地漏不得对所生产的产品产生污染。100级洁净室(区)内不得设置地漏,操作人员不应裸手操作,当不可避免时,手部应及时消毒。
1.2.13 10000级洁净室(区)使用的传输设备不得穿越较低级别区域。
1.2.14 100000级以上的洁净工作服应在洁净室(区)内洗涤、干燥、整理,必要时应按要求灭菌。
1.3 设备的要求
用于生产和检测的仪器、仪表、量具、衡器等,其适用范围和精密度应符合生产和检验要求,有明显的合格标志,并定期校验。
2、检测方法
2.1 温湿度的检测
2.1.1 测试之前空气净化系统应至少已连续运行24小时,且系统处于稳定和正常运行的状态,测试人员在采样时也应注意站在测试仪器的下风侧,并应尽量少活动;
2.1.2 若局部为恒温恒湿区域,则必须在测试记录中注明,并按规定布置采样点和计算偏差,采样点布置如下∶若非恒温恒湿洁净室(区),则采样点为离地0.8m、距墙0.5m的室内中心位置;若为恒温恒湿度洁净室(区),则应符合以下规定∶
a∶ 每次测试间隔不大于30分钟,并不少于48小时;
b∶ 室内采样点布置应包括送回风口处、恒温工作区具有代表性的地点(例如沿着工艺设备周围布置或等距离布置);
c∶ 采样点一般应布置在距墙面大于0.5m,离地面0.8m的同一高度上,也可以根据恒温区的大小,分别布置在离地不同高度的几个平面上;
d∶采样点数应符合表1规定∶
表1 温度与相对湿度采样点数
波动范围 | 室面积≤50㎡ | 每增加20~50m2 |
Δt=±0.5℃~±2℃ | 5个 | 增加 3~5个 |
ΔRH=±5%~±10% | ||
Δt≤±0.5℃ | 点间距不应大于2m,点数不应少于3个 | |
△RH≤±5% | ||
2.1.3 采用直接读数法,从而评定该洁净室(区)的温度与相对湿度。若使用电子元件支持的数字式温度与相对湿度计,则仪器开机预热至稳定后,方可按仪器说明书的规定对仪器进行校正,并选定相应的测试量程范围,宜将温度和相对湿度计的测试探头尽量与采样点保持水平面一致,在确认读数稳定后方可开始测试;
2.1.4 应同时测试室外的温度和相对湿度值;
2.1.5 对于无恒温恒湿要求的洁净室(区),温度与相对湿度的采样数据与标准对比后得出合格与否的结论。对于有恒温恒湿要求的洁净室(区),判断温度与相对湿度是否符合标准应同时满足∶ 室温波动范围与各采样点的各次温度测试数据中偏差控制点温度的最大值一致,占采样点总数的百分比整理成累积统计曲线,若 90%以上的采样点的偏差值在室温波动范围内,则为符合规定,反之则不合格,相对湿度的波动范围可按室温波动范围的规定执行;
2.1.6 若同时测试两个项目以上时,温度和相对湿度的测试宜在最先进行,有利于综合评估温度与相对湿度对其他项目的影响; 太低的相对湿度会导致静电问题,使灰尘吸附在金属表面,而相对湿度过高时,微生物污染的风险显著增大;对于洁净室(区)的加湿处理,应使用高质量的水以避免污染。
2.2 换气次数的检测
2.2.1 对于非单向流洁净室(区),对每个送风口测试送风量来换算出换气次数。换气次数的计算公式如下∶

2.2.2 采用空气平衡热辐射测量仪或风量罩,直接读出每个送风口的送风量值(m2/h),洁净室(区)内所有送风口的送风量之和即为洁净室(区)送风量;
2.2.3 对于非单向流洁净室(区),也可采用风口法或风管法确定送风量, 方法如下;
a: 风口法是在安装有高效过滤器的送风口处,根据送风口形状连接辅助风管进行测量。即用镀锌钢板或其他不产尘材料做成与风口形状及内截面相同,长度等于2 倍风口长边长的直管段,连接于风口外部,在辅助风管的出口平面上,按最小采样点数不小于 6 点均匀布置采样点,用风速仪测定各采样点风速。采样点范围为送风口边界内 0.05m 以内的面积,以所有采样点风速读数的算术平均值作为平均风速;然后,以送风口截面平均风速乘以送风口净截面积求取风量;
b: 对于风口上风侧有较长的矩形支管段,目已经或可以钻孔时, 可以用风管法确定风
量。测量断面应位于大于或等于局部阻力部件前 3 倍管径或管径长边长的部位,也可以是局部阻力部件后5倍管径或管径长边长的部位,对于圆形风管,应根据管径大小将截面划分成若干个面积相同的同心圆环,每个圆环设4 个采样点,圆环数量宜不少于3个,以所有采样点风速读数的算术平均值作为平均风速,对于矩形风管,可将风管截面划分成若干个相等的小截面,每个小截面尽可能接近正方形,边长最好不大于 200mm,以每个正方形的中心点作为采样点测试风速值,但整个截面上的采样点数不少于 3 个,以所有采样点风速读数的算术平均值作为平均风速;然后,以送风口截面平均风速乘以送风口净截面积求取送风量;
截面平均风速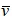 :
:
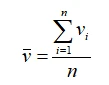
式中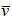 为截面平均风速,m/s;
为截面平均风速,m/s;
Vi为某一采样点的风速(i=1,2,...,n),m/s;
n为采样次数,次。
某一送风口的送风量S:
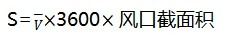
2.2.4 测试数据经过计算整理后,与标准值比较后得出结论。
2.3 截面平均风速的检测
采用风速计直接测试。风速为(0.36~0.54)m/s(指导值)。
2.3.1 对于垂直单向流洁净室,测试时取离高效过滤器0.3m垂直于气流处的截面作为采样截面,对于水平单向流洁净室,测试时采样点应取在距送风面0.5m的垂直截面上,截面上的采样点间距不宜大于0.6m,均匀布点;采样点数应不少于5个;
2.3.2 测试风速时,宜用测定架固定风速仪,以避免人体干扰;;若不得不用手持风速仪测试时,手臂应伸至最长位置,尽量使人体远离采样点;在具体操作时要注意的是,测试截面风速时测试仪器的测试元件前后不能有遮挡物,否则就会导致数据失准或者无法测出风速;
2.3.3 以所有测点的风速读数的算术平均值作为截面平均风速,并以截面平均风速的数值与标准对比得出合格与否的结论。截面平均风速,按本标准"测试方法"项下第(2)项"换气次数的测试"中的“截面平均风速![]() ”进行;
”进行;
2.3.4 截面风速不均匀度 βV应按下式计算∶
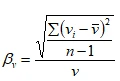
式中 βv,为截面风速不均匀度;
vi为某一采样点的风速(i=1,2,…,n),m /s;
n为采样次数,次;
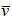 为截面平均风速∶ m /s;
为截面平均风速∶ m /s;
截面风速不均匀度βV不大于0.25。
2.4 静压差和压差梯度的检测
压差测试应在风量平衡调节完毕后进行。为了测量相邻区域的压差,在整个测试过程中
用微压差计进行测量。测量时必须把所有门全部关紧,然后从洁净室的最里面逐步向外测量,
每一个房间相对于所有其他房间或区域的压差均应测量,在测量时应特别注意每一个测点与
其相邻位置压差的方向,同时在气流流向图上标明压差梯度。
如果相邻两个房间或区域之间的压差有接受标准,则用具体数值表示,无压差要求则用""表示;"+"则表示"房间"的压力高于"相对位置"的区域;"一"则表示"房间"的压力低于"相对位置"的区域。测试时应尽量远离送风口和回风口或其他可以影响压差测量的因素。有不可关闭的开口与邻室相通的洁净室,还应测试开口处的两端压差,气流流速和气流流型等。
2.4.1 若使用指针型微压差计,则采用直接读数法,并根据测试的压差值评定该洁净室(区)
与相邻区域的气体压力,若使用其他微压差计,则应先调整水平,确认符合后方可进行,若使用电子元件支持的数字式微压差计,则仪器开机预热至稳定后,方可按说明书的规定对仪器进行校正,并选定相应的测试量程范围;
2.4.2 若可能,宜将微压差计的连接管尽量与采样点水平面一致,采样点位置离地约0.8m高度的水平面上,选择在无涡流无回风口的位置,在确认读数稳定后可开始测试;
2.4.3 压差值的采样数据与标准比较得出合格与否的结论,测试压差的同时应结合被测洁净室(区)的换气次数或截面风速的测试,有利于对洁净室(区)进行综合评价,A级(ISO Class 5)以上洁净级别的洁净室(区)在开门时,若必需,则要监控门内0.6m 处的悬浮粒子的浓度。
2.5 悬浮粒子的检测
采用计数浓度法,即通过测定洁净环境内单位体积空气中含大于或等于某粒径的悬浮粒子数,来评定该洁净室(区)的洁净度等级。测试方法采用ISO 14644.1《Cleanrooms and associated controlled environments-Part 1 Classification of air cleanliness》以及 GB/T 16292-2010《医药工业洁净室(区)悬浮粒子的测试方法》。为确认A级洁净区的级别,每个采样点的采样量不得少于1立方米。A级洁净区空气悬浮粒子的级别为ISO4.8,以≥5.0μm的悬浮粒子为限度标准。B级洁净区(静态)的空气悬浮粒子的级别为 ISO 5,同时包括表中两种粒径的悬浮粒子。对于C级洁净区(静态和动态)而言,空气悬浮粒子的级别分别为 ISO7和ISO8。对于D 级洁净区(静态)空气悬浮粒子的级别为ISO8。
测试方法如下∶
2.5.1 最少采样点数量NL∶
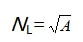
式中NL为最少采样点;
A 为洁净室或被控洁净区的面积,㎡。
注∶在水平单向流情况下,面积A为垂直于气流方向的横截面积。
静态测试时,采样点离地面 0.8m 高度的水平面上均匀布置。每点采样2~3次。
2.5.2 结果计算∶
采样点的平均悬浮粒子浓度∶

式中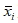 为某一采样点的平均粒子浓度,粒/m3;
为某一采样点的平均粒子浓度,粒/m3;
 为某一采样点的粒子浓度(i=1,2,...,n),粒/m3;
为某一采样点的粒子浓度(i=1,2,...,n),粒/m3;
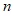 为某一采样点的采样次数,次。
为某一采样点的采样次数,次。
平均值的均值:

式中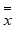 为平均值的均值,即洁净室(区)的平均粒子浓度,粒/m3;
为平均值的均值,即洁净室(区)的平均粒子浓度,粒/m3;
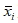 为某一采样点的平均粒子浓度(i=1,2,...,L),粒/m3;
为某一采样点的平均粒子浓度(i=1,2,...,L),粒/m3;
m为某一洁净室(区)的总采样点数,个。
标准差s:

式中 s为平均值均值的标准误差,粒/m3。
95%置信上限(95%UCL):

式中 95%UCL为平均值均值的95%置信上限,粒/m3;
t0.95为95%置信上限的t分布系数,见下表。
表2 95%置信上限的t分布系数:
采样点数m | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | >9 |
t | 6.3 | 2.9 | 2.4 | 2.1 | 2.0 | 1.9 | 1.9 | 1.9 | - |
注:当采样点数多于9点时,不需要计算95%UCL | |||||||||
2.5.3 接受标准为同时满足以下两条:
a:每个采样点的平均悬浮粒子浓度不得大于规定的级别界限,即![]() ≤级别界限;
≤级别界限;
b:全部采样点的悬浮粒子浓度平均值均值的95%置信上限必须不大于规定的级别界限,即UCL≤级别界限。
2.5.4 任何洁净室(区)的采样点不得少于2个,每个选定的采样点至少采样一次,在一个区域内至少采样5次,不同采样点的采样次数可以不同,工作区的采样点位置宜在离地0.8m高度的水平面上,采样点多于5点时,也可以在离地面0.8~1.5m 高度的区域内分层布置,但每层不少于5点;
2.5.5 采样管必须干净,连接处不得有渗漏,采样管的长度应根据允许长度确定,如果无规定时,不宜大于1.5m。对于单向流洁净室(区),粒子计数器的采样管口朝向应正对气流方向,对于非单向流洁净室(区),采样器的采样管口向上,采样时应适当避开尘粒较集中的回风口,测试人员在采样时也应在粒子计数器采样管口的下风侧,并尽量少活动;
2.5.6 采样管口置于采样点采样时,宜在粒子计数器确认计数稳定后方可开始连续读数,粒子计数器的采样管口与仪器工作位置宜处在同一气压和温度下,以免产生测量误差,采样完毕后,仪器须自净;
2.5.7 应采取一切措施防止采样过程的污染。静态测试时采样点可遵循均匀布置的原则,同时根据相应的法洁净度级别开展风险评估,确定动态监测的采样点位置并推荐进行日常动态监控。
2.5.8 若同时测试两个以上项目时,悬浮粒子的测试宜在温度和相对湿度、送风量(换气次数)、压差等项目结束后进行,以降低干扰。
2.6 浮游菌的检测
采用计数浓度法。即通过收集悬浮在空气中的生物性粒子于专门的培养基(选择能证实其能够支持微生物生长的培养基),经若干时间和适宜的生长条件让其繁殖到可见的菌落计
数,以判定该洁净室的微生物浓度。测试方法采用 GB/T16293-2010《医药工业洁净室(区)浮游菌的测试方法》。
若被测区域为洁净度A级洁净区(静态或动态),B级洁净区(静态)应满足每个采样点的最小采样量不小于1立方米,应满足最少采样点和每个采样点的最小采样量的规定。
2.6.1 最少采样点数量NL∶
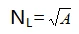
式中NL为最少采样点;
A为洁净室或被控洁净区的面积,㎡。
静态测试时,采样点离地面 0.8m 高度的水平面上均匀布置。每点采样1~2次。同时根据相应的洁净度级别开展风险评估。 确定动态监测的采样点位置并推荐进行日常动态监控
2.6.2 浮游菌采样器一般采用撞击法机理,可分为狭缝式、离心式或针孔式采样器。狭缝式采样器由附加的真空抽气泵抽气,通过采样器的狭缝式平板,将采集的空气喷射并撞击到缓慢旋转的平板培养基表面上,附着的活微生物粒子经培养后形成菌落。离心式采样器由于内部风机的高速旋转,气流从采样器前部吸入从后部流出,在离心力的作用下,空气中的活
微生物粒子有足够的时间撞击到专用的圆形培养皿上,附着的活微生物粒子经培养后形成菌落。针孔式采样器是气流通过一个金属盖吸入,盖子上是密集的经过机械加工的特制小孔,通过风机将收集到的细小的空气流直接撞击到平板培养基表面上,附着的活微生物粒子经培养后形成菌落;
2.6.3 浮游菌采样器一般采用φ150mm×15mm、φ90mm×15mm、φ65mm×15mm等规格的平板培养皿,也可根据所选用的采样器选择合适的培养皿。培养基为肉汤琼脂培养基或其他《中国药典》认可的培养基。恒温培养箱∶必须是定期检定的满足相应的培养温度及精度要求的培养箱;
2.6.4 培养基的准备及灭菌∶一般采用商品脱水培养基,临用时按照使用说明书进行配制,并调节pH值使灭菌后培养基的pH值符合规定。若为自制培养基,原料应挑选,琼脂凝固力应测定,以决定配制时的琼脂用量,试剂规格应为化学纯以上。培养基配制后应在2小时
内按《中国药典》规定的方法灭菌,避免细菌繁殖;
2.6.5 培养皿的制备∶空白培养皿在注入培养基前应为无菌状态,然后将配制灭菌后的培养基加热熔化,冷却至45℃左右时,在无菌操作的要求下将培养基注入培养皿,直径为150mm 的培养皿不少于60ml培养基,直径为90mm的培养皿不少于20ml培养基;
2.6.6 培养皿使用前的培养∶待琼脂凝固后,将培养皿倒置于30~35℃的恒温培养箱中培养 48小时以上,若培养皿上确无菌落生长,即可供采样用;
2.6.7 对于单向流洁净室(区),采样器的采样管口朝向应正对气流方向,对于非单向流洁净室(区),采样器的采样管口向上,采样时应适当避开尘粒较集中的回风口,测试人员在采样时也应站在采样器采样管口的下风侧;
2.6.8 应采取一切措施防止采样过程的污染和其他对样本可能的污染。测试状态有静态和动态两种,必须在测试记录中注明;
2.6.9 在进行测试之前,应先对所用的培养皿进行检查,确认没有气泡、无凹陷、无细菌生长并在使用有效期内;培养皿在使用前必须用消毒剂擦净外表面;
2.6.10 采样器的采样头及盖子应采用可以灭菌的材料,在进入洁净室(区)测试前也应采用适当方式消毒。若必须进入A级洁净室(区)采样,整个设备要有措施保护,然后才能带入相关洁净室(区)。在开始采样准备前,采样器的采样头的内外表面宜用消毒剂擦拭,狭缝式和离心式采样器应检查采样器的采样管,严禁渗漏,内壁应光滑,采样管应尽量减少弯曲,采样管的内外壁都要消毒,检查采样器的流量显示,并选定合适的采样时间,仪器在消毒后,先不放入培养皿,开启采样器一段时间驱赶消毒剂的残留物;
2.6.11 测试人员在采样时应避免接触采样头和采样管的内表面,在采样器内放入培养皿后,取下培养皿的盖子,避免被水滴或其他浮游物质污染,然后开启采样器;采样过程结束后,盖上培养皿的盖子,取下培养皿,在采样器上调换培养皿时,测试人员宜双手消毒,也可戴无菌手套操作,每一个培养皿上都应作标识;
2.6.12 全部采样结束后,将培养皿倒置于恒温培养箱中培养。采用大豆酪蛋白琼脂培养基(TSA)配制的培养皿经采样后,在30~35℃培养箱中培养,时间不少于2天,采用沙氏培养基(SDA)配制的培养皿经采样后,在20~25℃培养箱中培养,时间不少干5天。每批培养基应有对照试验,检验培养基本身是否污染。可每批选定3只培养皿作对照培养。用肉眼对培养皿上所有的菌落直接计数、标记或在菌落计数器上点计,然后用5~10 倍放大镜检查,有否遗漏。若平板上有2个或2个以上的菌落重叠,可分辨时仍以2个或2个以上菌落;
2.6.13 用计数方法得出各个培养皿的菌落数后,用下式计算每个采样点浮游菌的平均浓度:
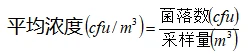
若某个采样点的平均浓度大于级别上限,则必须对该区域重新消毒,再采样2次,2次必须均合格后才能判定合格;
2.6.14 对于浮游菌的监控,应采用基于风险的原则设定纠偏限度和警戒限度,以保证洁净室(区)的微生物浓度受到控制,操作规程中应当详细说明结果超标时需采取的纠偏措施。应定期测试以检查微生物负荷以及消毒剂的效力,并作趋势分析。静态和动态的监控都可以采用以上方法;
2.6.15 若同时测试两个以上项目时,浮游菌浓度的测试宜在其他项目结束后进行,以降低干扰;
2.6.16 培养皿在用于测试时,宜同时进行空白试验校正,避免培养皿运输或搬动过程造成的影响。每次或每个区域取1个对照皿,然后与采样后的培养皿(肉汤琼脂)一起放入35℃±2℃的培养箱内培养48小时以上,结果应无细菌生长;
2.6.17 浮游菌采样时,由于气流以每秒几十米的速度从缝隙或细孔中吹向培养基表面,时间过久就会使培养基水分减少导致灵敏度降低,因此采样时间宜控制在20分钟之内。
2.7 沉降菌的检测
采用沉降法,即通过自然沉降原理收集空气中的生物性粒子于培养皿(选择能证实其能够支持微生物生长的培养基),经若干时间和适宜的生长条件让其繁殖到形成一个个独立可见的菌落为计数依据,以判定该洁净室(区)的微生物浓度。
2.7.1 沉降菌测试一般采用φ90mm×15mm、φ65mm×15mm等规格的平板培养皿,也可根据工艺要求选择合适的培养皿。
2.7.2 培养基的准备及灭菌、培养皿的制备、培养皿使用前的培养采用与"浮游菌的检测"相同的方法制备。
2.7.3 静态测试时洁净室(区)沉降菌采样点的布置应遵循均匀全面的原则,避免采样点在某局部区域过于集中,除非是为了特殊的目的。工作区的采样点位置离地0.8~1.5m左右,离开送风面30cm以上,动态测试时也可在关键设备或关键工序处增加采样点。采样点的位置可以与悬浮粒子的采样点相同,每个采样点至少采样一次。
2.7.4 对于单向流洁净室(区),采样时应正对气流方向,对于非单向流洁净室(区),采样时培养基平皿打开向上,采样时应适当避开尘粒较集中的回风口,测试人员在采样时也应站在采样器采样管口的下风侧;
2.7.5 在进行测试之前,应先对所用的培养皿进行检查,确认没有气泡、无凹陷、无细菌生长并在使用有效期内,培养皿在使用前必须用消毒剂擦净外表面;
2.7.6 应采取一切措施防止采样过程的污染和其他对样本可能的污染。静态测试时,室内测试人员不得多于2人。沉降菌采样时应按事先确定的采样点位置从里到外放置好培养皿,然后从里到外取下培养皿的盖子,同时避免被水滴或其他浮游物质污染,采样过程结束后,从外到里盖上培养皿的盖子,也可带无菌手套操作,每一个培养皿上都应作标识;
2.7.7 全部采样结束后,将培养皿倒置于恒温培养箱中培养。采用大豆酪蛋白琼脂培养基(TSA)配制的培养皿经采样后,在30~35℃培养箱中培养,时间不少于2天;采用沙氏培养基(SDA)配制的培养皿经采样后,在20~25℃培养箱中培养,时间不少于5天。每批培养基应有对照试验,检验培养基本身是否污染。可每批选定3只培养皿作对照培养。用肉眼对培养皿上所有的菌落直接计数、标记或在菌落计数器上点计,然后用5~10倍放大镜检查,有否遗漏。若平板上有2个或2个以上的菌落重叠,可分辨时仍以2个或2个以上菌落计数;
2.7.8 用计数方法得出各个培养基平皿的菌落数后,用下式计算沉降菌的平均浓度:
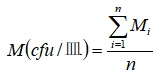
式中 M为平均菌落数: cfu/皿;
Mi为某一编号培养皿的菌落数:cfu/皿;
n为培养皿总数
2.7.9 对于沉降菌的监控,应采用基于风险的原则设定纠偏限度和警戒限度,以保证洁净室(区)的微生物数量受到控制,操作规程中应当详细说明结果超标时需采取的纠偏措施。应定期测试以检查微生物负荷以及消毒剂的效力,并作趋势分析。静态和动态的监控都可以采用以上方法;
2.7.10 若同时测试两个以上项目时,沉降菌浓度的测试宜在其他项目结束后进行,以降低干扰;沉降菌测试时,在放置培养皿时应注意尽量防止人员走动引起的气流扰动影响检测结果;
2.7.11 培养皿在用于测试时,宜同时进行空白试验校正,避免培养皿运输或搬动过程造成的影响。每次或每个区域取1个对照皿,然后与采样后的培养皿(肉汤琼脂)一起放入35℃±2℃的培养箱内培养48小时以上,结果应无细菌生长。
2.8 照度、最低照度及照度均匀度的检测
照度值为被测洁净室(区)的室内最低照度值。采用直接读数法,即通过测定洁净环境内各点的照度值,并从中筛选出最低照度值,从而评定该洁净室(区)的照度。若必需,也可根据测试的照度值计算出照度均匀度。
2.8.1 照度测试应在光源输出趋于稳定,并尽量避开自然采光的情况下进行,若有局部照明,则必须在测试记录中注明动态测试时的局部照明位置和局部照明的照度值,照度测试时应确认所有光源的工作状态处于正常,否则必须详细记录光源状况,应注意测试者的投影以及服装的反射影响测试结果;
2.8.2 应在测试出被测洁净室(区)的温度值后再进行照度测试。照度测试仪器开机、预热至稳定后,方可按说明书的规定对仪器进行校正,并选定相应的测试量程范围;
2.8.3 应将照度计的受光面尽量与测试点相应水平面一致,在确认读数稳定后方可开始测试;
2.8.4 照度测试时的采样点布置:任何洁净室(区)的采样点不得少于2个,除受洁净室(区)内的设备限制之外,采样点应在整个洁净室(区)内均匀布置,采样点距墙1m(小面积房间0.5m),按1~2m间距布点。每个选定的采样点之间间距不超过2m,不刻意在灯下或避开灯下选点,至少采样一次,在一个区域内至少采样5次,不同采样点的采样次数可以不同。如无特别规定,采样点置于离地0.8m高度的水平面上,若以室内工作台为对象面时,测试面定为其面上0.05m的水平面;
2.8.5 最低照度值的采样数据应按下述步骤进行统计计算:
B=Amin
式中 B为洁净室(区)的照度值,lx;
Amin为某一采样点的最低照度值(i=1,2,…,N),lx;
照度均匀度按下述步骤进行统计计算∶
平均照度BAvg:
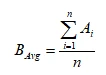
式中 BAvg为平均照度,lx;
Ai为某一采样点的照度(i=1,2,…,n),m /s;
n为采样次数,次。
照度均匀度B均∶
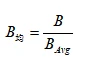
2.8.6 判断照度是否符合标准应同时满足∶
a: 洁净室(区)内主要工作区的最低照度值必须大于规定的范围,即B≥300lx;有局部照明的除外;
b: 若必须,洁净室(区)内主要工作区的照度均匀度宜大于0.7;
2.8.7 备用照明和应急照明的测试不在本标准规定的范围内。